1. 引言
人造金红石是一种重要的钛产业基础原料,主要用于生产氯化法钛白粉、海绵钛、四氯化钛及电焊条药皮,是天然金红石的优秀替代产品 [1]。在人造金红石不同的生产工艺路线中,盐酸浸出法生产工艺具有浸出速度快、除杂能力强、产品质量高,适合处理各种类型矿源等优点而成为主流工艺,并很早就实现了工业化 [2] [3] [4] [5]。但是使用盐酸作为浸出反应的除杂剂,为了获得品位较高的人造金红石,反应需要加入的盐酸必然过量,在反应完成后,浸出液中含有大量的游离盐酸,同时钛精矿中除钛以外的金属氧化物与盐酸反应进入溶液内,形成大量氯化物,其处理相当困难,国外生产企业借鉴钢铁酸洗生产线废母液处理采用酸再生技术对盐酸再生循环使用,但需要大量投资建设。
在聚合氯化铁混凝剂中引入铝盐,能够起到综合铁盐和铝盐两种混凝剂的优点,克服铁盐的出水不清、色度高、稳定性差和铝盐矾花生成速度慢、质量轻等缺点,具备比单一铁盐或铝盐更优良的混凝性能 [6] [7] [8],而在采用盐酸浸出钛精矿法中,由于钛精矿中本身含有氧化铝,经过浸出处理后进入液相,浸出母液经过氧化后聚合,在氯化铁聚合的同时,钛精矿浸出产生的氯化铝一并聚合,形成含铝的聚合氯化铁混凝剂,由于铝的存在,聚合得到混凝剂,稳定性得到提高,同时净化效果获得提高。直接使用人造金红石浸出母液制备获得含铝聚合氯化铁混凝剂,考察对生活污水的处理效果。
2. 材料与方法
2.1. 仪器与原料
主要仪器:电子恒温水浴锅;电动搅拌器;三口烧瓶;便携式浊度仪。
主要原料:人造金红石浸出废液;氯气(Cl2 ≥ 99.5%);氢氧化钠(NaOH, 48%);盐酸(HCl ≥ 31%);上述原料均来自宜宾海丰和锐有限公司;铁粉(Fe ≥ 99%),中国冶金研究总院。
2.2. 混凝剂制备
2.2.1. 含铝聚合氯化铁
取100 mL钛精矿盐酸浸出母液(化学成分见表1)于三口烧瓶中并置于水浴锅内,在通风橱内开展实验,在25℃和100 r/min搅拌条件下,定量分批通入氯气作为氧化剂,将二价铁离子氧化为三价铁离子后,搅拌反应1 h,缓慢加入10% NaOH溶液,搅拌反应后即得液体含铝聚合氯化铁混凝剂。
2.2.2. 聚合氯化铁
取100 g铁粉与31%盐酸500 g置于1 L烧杯中混合搅拌反应8 h,过滤去除不溶物得酸性FeCl2溶液,对酸性FeCl2溶液进行冷冻结晶处理,冷冻后分离得到FeCl2含水结晶体。
取100 mL FeCl2溶液于三口烧瓶中并置于水浴锅内,在通风橱内开展实验,在25℃和100 r/min搅拌条件下,定量分批通入氯气将二价铁离子氧化为三价铁离子,搅拌反应1 h后缓慢加入10% NaOH溶液,搅拌反应后即得液体聚合氯化铁混凝剂。
2.3. 氧化率
式中:m1:氧化前溶液中二价铁含量;
m2:氧化后溶液中二价铁含量;
溶液中二价铁含量采用容量分析。
3. 结果及讨论
3.1. 钛精矿的选择
钛元素在自然界主要以二氧化钛或含氧酸盐的形式存在,含氧酸盐主要是含铁钛酸盐。当前具有开采价值钛矿床一般分为岩矿型和砂矿型,岩矿型钛矿是原生矿,如我国攀西钒钛磁铁矿,其主要矿物为钛磁铁矿和赤铁矿,含有钒、钴、镍、铜和铬等金属元素。砂矿型钛矿属于次生矿,来源于岩矿型钛矿的蚀变,内陆地表暴露的岩矿型钛矿受到风化、雨水侵蚀等作用,由致密岩矿型逐渐转变为颗粒相对细小的砂矿,并在雨水和风力的作用下沉积于河流、山谷低处及盆地,如我国云南的砂矿及澳大利亚柏斯盆地砂矿;沿海砂矿型钛矿主要是由内陆钛矿随水流富集在沿海,如莫桑比克东部沿海钛砂矿。
钛矿在蚀变的过程中不仅发生粒度变化,还伴随一些组分溶出,随着铁的氧化和溶蚀,所含的钙、镁在侵蚀过程中含量降低,TiO2得到富集,但是对于以固溶体形式与TiO2结合的有色金属离子,通过选矿方式很难将其选别。此外,砂矿型钛矿也常与其他矿物伴生,除了含有钛铁矿、金红石、锆钛矿等矿物外,常含具有放射性的独居石,以及风化过程中吸附在钛铁矿晶体表面的铀和钍,采用此类钛铁矿作为制人造金红石的原料,放射性元素将在酸浸过程中进入溶液,成为环境污染的潜在威胁。攀西钛精矿与南非钛精矿的典型成分见表1。

Table 1. Typical composition of Panxi and South African titanium concentrate
表1. 攀西钛精矿与南非钛精矿的典型成分(%)
选择岩矿型的攀西钛精矿作为原料生产人造金红石时,原料中不含对水质产生严重影响的重金属离子和放射性元素,浸出母液是一种较好的制备水处理剂原料,利用其中的铁,经过聚合形成多聚物,用于污水处理,使用国内攀西钛精矿浸出后的母液为原料,浸出母液成分见表2。

Table 2. The composition of the artificial rutile by-product acid waste liquid
表2. 人造金红石母液成分(g/L)
3.2. 氧化剂的选择
制备聚合氯化铁关键是氧化,其原理为在酸性溶液中投加氧化剂将亚铁离子转化为铁离子,再经过水解、聚合反应得到聚合氯化铁。在工业上常使用的能够氧化亚铁的氧化剂有:氯气、氯酸钠、次氯酸
钠、双氧水、硝酸等。
、
、
、
、
而
,次氯酸钠和硝酸虽然氧化电位高于铁,能够氧化,但是相差
不大,氧化时会出现氧化不充分,氯酸钠氧化性强,但属于易爆试剂,工业上运输和使用要求严格,存在安全风险。双氧水氧化后生成水,是一种较好的无污染氧化剂,但有效氧化成分含量低,含大量水,使用时会将聚合氯化铁稀释。氯气属于危化品,但工业上有成熟工艺将其液化后进行罐装运输,使用时将液氯蒸发为气体使用,且氯气也是一种水质净化处理剂,特别适宜于与氯碱行业联合生产厂使用,我公司作为氯碱行业企业,对氯气的使用及安全防范准备充分,具备使用氯气开展实验的条件,因此选用氯气作为氧化剂。
3.3. 通入氯气速率
量取100 mL人造金红石浸出母液于250 mL烧杯中,在通风橱内、室温并搅拌条件下按不同速率鼓入1 L氯气(根据溶液二价铁含量计算,1 L氯气不能将二价铁氧化完全),通完氯气后继续搅拌反应15 min,再测定溶液中Fe2+含量,并计算其转化率,不同氯气通入速率对Fe2+氧化率的影响如图1。
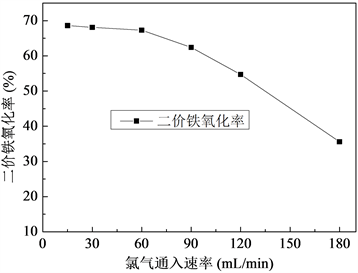
Figure 1. Effect of chlorine gas pass rate on Fe2+ oxidation rate
图1. 氯气通入速率对Fe2+氧化率的影响
由图1可知,氯气通入速率对二级铁的氧化影响较大,通入氯气速率较慢时,二价铁氧化较完全,二价铁氧化率接近理论氧化值,当氯气通入速率高于60 mL/min后,二价铁氧化率降低幅度较大,归因于氯气通入速率较快,导致氯气不能与人造金红石浸出母液中的二价铁及水充分反应,为保证氯气充分发挥氧化作用,后续实验拟采用60 mL/min的通入速率。
3.4. 氯气加入量
量取100 mL人造金红石浸出母液于250 mL烧杯中,在通风橱内、室温并搅拌条件下,以60 mL/min的速率缓慢鼓入氯气,继续反应15 min后,测定溶液中Fe2+含量,并计算其转化率,结果见图2。
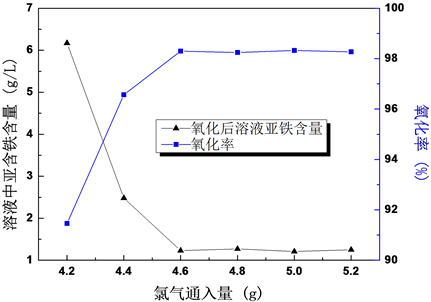
Figure 2. Effect of chlorine volume on ferrous oxidation insolution
图2. 氯气通入量对溶液亚铁氧化影响
由图2可知:氯气通入量对于氧化效率影响较大,在氯气通入量小于4.4 g时,随着氯气的通入,反应后溶液中Fe2+含量迅速减少,转化率快速提高;当氯气通入量达到4.6 g后,溶液中的Fe2+转化率基本不变,表明氧化反应达到平衡,及氯气在达到稍过量情况下氧化反应完成,若继续通入氯气,通入的氯气溢出溶液,此时有较为浓烈的氯气味,表明氯气过量未与溶液中Fe2+反应,因此确定氯气通入量为4.6 g。
3.5. 氧化温度
量取100 mL人造金红石浸出母液于250 mL烧杯中,在通风橱内、放置于不同恒温水浴锅内,以60 mL/min的速率缓慢鼓入氯气,继续反应15 min后,测定溶液中Fe2+含量,并计算其转化率,结果见图3。

Figure 3. Effect of oxidation temperature on ferrous content
图3. 氧化温度对亚铁含量的影响
由图3可知:在室温条件下通入氯气,氯气迅速与溶液中亚铁反应,随着温度升高,反应体系温度达到30℃以上,氯气与溶液中亚铁反应处于平衡状态,主要是氯气在溶液中溶解、反应处于平衡,随着温度升高,其在溶液中溶解减少,反应速度增加,但易从水中溢出,形成氯气脱离液相,因此温度选择室温条件下进行。
3.6. 氧化反应时间
量取100 mL人造金红石浸出母液于250 mL烧杯中,在通风橱内、在室温条件下,并搅拌条件下缓慢鼓入氯气4.6 g,鼓入氯气时间为20 min,然后放置不同时间进行进一步氧化反应,测定溶液中Fe2+含量,并计算其转化率,结果见图4。
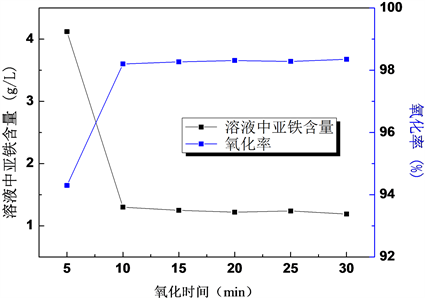
Figure 4. Effect of oxidation time on ferrous content
图4. 氧化时间对亚铁含量的影响
图4数据表明:在浸出母液中通入氯气后,亚铁得到迅速氧化,氧化时间达到10 min后,亚铁转化率基本不变,达到98%以上,实验中采用通入氯气氧化10 min后即可进行聚合操作。
4. 产品性能指标
实验室自制的聚合氯化铁与市场上的聚合氯化铁产品指标见表3。

Table 3. Polyferric chloride product index
表3. 聚合氯化铁产品指标
5. 混凝性能比较
为了进一步研究制备获得的含铝聚合氯化铁的混凝性能,使用盐酸与铁粉反应,结晶制备获得氯化亚铁,按照选择的试验条件制备聚合氯化铁和母液制备的含铝聚合氯化铁以及外购聚合氯化铁,使用高岭土溶液浊度去除率对混凝剂净化效果进行测试,结果见图5 (投药量以铁计)。
对使用自制结晶后的氯化亚铁制备聚合氯化铁和母液制备含铝聚合氯化铁,稳定性在熟化后,采用静置放置模式考察稳定性,氯化亚铁制备得到的聚合氯化铁24 h后开始分层,采用母液制备的含铝聚合氯化铁放置一周后才开始出现分层现象,稳定性增加,主要是由于在浸出母液中含有铝,铁聚合时铝一并发生聚合,由于铝的存在,聚合物溶液稳定性增加,同时在混凝时铁和铝的协同效应,其含铝聚合氯化铁除浊效果好。

Figure 5. Turbidity removal effect of coagulant
图5. 混凝剂除浊效果
6. 结论
1) 采用攀西钛精矿生产人造金红石产生的母液,由于其中矿石与砂矿相比,不含重金属和放射性元素,母液中含有大量铁,是一种制备聚合氯化铁的较好原料,能够很好处理浸出母液,资源综合利用,能有效改善人造金红石经济效益。
2) 使用氯气作为母液中亚铁氧化剂,制备得到聚合氯化铁,用于污水处理,制备流程短,处理简单。
3) 相比于聚合氯化铁,采用攀西钛精矿生产人造金红石副产母液制备的含铝聚合氯化铁,处理污水除浊效果更好。