Abstract
τ-Fluvalinate residues in bees, honey and wax were measured in two experimental hives treated with Apistan to test a multi-compartmental predictive model. Pesticide residues were monitored for 30 days after treatment in bees and for up to 180 days in honey and wax. Concentrations ranged between 14 and 160 ng g−1 f.w. in bees and between 98 and 1630 ng g−1 in wax, while no residues were detected above the analytical limit (2.5 ng g−1) in honey. τ-Fluvalinate residues are discussed in the context of a survey of data from the literature on other pesticides (bromopropylate, coumaphos, malathion and amitraz). This data review shows that residues of the same compound exhibit extremely high variability within the same matrix. This finding underlines the importance of developing predictive tools for both post-treatment analysis and a priori evaluation of the possible contamination effects of pesticides depending on the mode of application.



Similar content being viewed by others
References
Bogdanov, S. (2006) Contaminants of bee products. Apidologie 37, 1–18
Bogdanov, S., Kilchenmann, V. (1995) Acaricide residues in beeswax: long-term studies in Switzerland. Apidologie 26, 319–321
Bogdanov, S., Kilchenmann, V., Imdorf, A. (1998) Acaricide residues in some bee products. J. Apic. Res. 37, 57–67
Bogdanov, S., Ryll, G., Roth, H. (2003) Pesticide residues in honey and beeswax produced in Switzerland. Apidologie 34, 484–485
Borneck, R., Merle, B. (1989) New tests for Varroa control with Apistan (fluvalinate). In: R. Cavalloro (ed.) Present status of varroatosis in Europe and progress in varroa mite control. Proc. Meet. EC expert Group, Udine, Italy, 28–30 November 1988, ECSC-EEC-EAEC, Brussels, pp. 315–330
Borneck, R., Merle, B. (1990) Experiments with Apistan in 1988. Apiacta 25, 15–24
Cabras, P., Floris, I., Garau, V.L., Melis, M., Prota, R. (1997) Fluvalinate content of Apistan® strips during treatment and efficacy in colonies containing sealed worker brood. Apidologie 28, 91–96
Chauvin, R. (1968) Traité de biologie de l’abeille, Masson et Cie, Paris
Chauzat, M.P., Faucon, J.P. (2007) Pesticide residues in beeswax samples collected from honey bee colonies (Apis mellifera L.) in France. Pest Manag. Sci. 63, 1100–1106
Chauzat, M.P., Faucon, J.P., Martel, A.C., Lachaize, J., Cougoule, N., Aubert, M. (2006) A survey of pesticide residues in pollen loads collected by honey bees in France. J. Econ. Entomol. 99, 253–262
Decourtye, A., Devillers, J., Genecque, E., Le Menach, K., Budzinski, H., Cluzeau, S., Pham-Delegue, M.H. (2005) Comparative sublethal toxicity of nine pesticides on olfactory learning performances of the honeybee Apis mellifera. Arch. Environ. Con. Tox. 48, 242–250
Feo, M.L., Eljarrat, E., Barceló, D. (2010) A rapid and sensitive analytical method for the determination of 14 pyrethroids in water samples. J. Chromatogr. A 1217, 2248–2253
Fernández, M., Pico, Y., Manes, J. (2002) Analytical methods for pesticide residue determination in bee products. J. Food Protect. 65, 1502–1511
Fernandez-Muiño, M.A., Sancho, M.T., Muniategui, S., Huidobro, J.F., Simal-Lozano, J. (1995) Acaricide residues in honey—analytical methods and levels found. J. Food Protect. 58, 449–454
Fernandez-Muiño, M.A., Sancho, M.T., Simal-Gandara, J., Creus-Vidal, J.M., Huidobro, J.F., Simal-Lozano, J. (1997) Acaricide residues in honeys from Galicia (NW Spain). J. Food Protect. 60, 78–80
Fries, I., Wallner, K., Rosenkranz, P. (1998) Effects on Varroa jacobsoni from acaricides in beeswax. J. Apic. Res. 37, 85–90
García, M.A., Fernández, M.I., Herrero, C., Melgar, M.J. (1996) Acaricide residue determination in honey. B. Environ. Contam. Tox. 56, 881–887
Ghini, S., Fernández, M., Picó, Y., Marín, R., Fini, F., Mañes, J., Girotti, S. (2004) Occurrence and distribution of pesticides in the Province of Bologna, Italy, using honeybees as bioindicators. B. Environ. Contam. Tox. 47, 479–488
Greatti, M., Milani, N., Nazzi, F. (1992) Reinfestation of an acaricide-treated apiary by Varroa jacobsoni Oud. Exp. Appl. Acarol. 16, 279–286
Halm, M.-P., Rortais, A., Arnold, G., Taséi, J.N., Rault, S. (2006) New risk assessment approach for systemic insecticides: the case of honey bees and imidacloprid (Gaucho). Environ. Sci. Technol. 40, 2448–2454
Haouar, M., Decormis, L., Rey, J. (1990) Fluvalinate applied to flowering apple trees—contamination of honey-gathering bees and hive products. Agronomie 10, 133–137
Jiménez, J.J., Bernal, J.L., del Nozal, M.J., Martin, M.T. (2005) Residues of organic contaminants in beeswax. Eur. J. Lipid Sci. Tech. 107, 896–902
Johnson, R.M., Ellis, M.D., Mullin, C.A., Frazier, M. (2010) Pesticides and honey bee toxicity—USA. Apidologie. doi:10.1051/apido/2010018
Kamel, A., Al-Ghamdi, A. (2006) Determination of acaricide residues in saudi Arabian honey and beeswax using solid phase extraction and gas chromatography. J. Environ. Sci. Heal. B 41, 159–165
Lodesani, M., Pellacani, A., Bergomi, S., Carpana, E., Rabitti, T., Lasagni, P. (1992) Residue determination for some products used against Varroa infestation in bees. Apidologie 23, 257–272
Lodesani, M., Costa, C., Bigliardi, M., Colombo, R. (2003) Acaricide residues in beewax and organic beekeeping. Apiacta 38, 31–33
Lodesani, M., Costa, C., Serra, G., Colombo, R., Sabatini, A.G. (2008) Acaricide residues in beeswax after conversion to organic beekeeping methods. Apidologie 39, 324–333
Mackay, D. (2001) Multimedia Environmental Model, The Fugacity Model, 2nd edn. Lewis Publisher, Boca Raton, Florida
Martel, A.C., Zeggane, S., Aurieres, C., Drajnudel, P., Faucon, J.P., Aubert, M. (2007) Acaricide residues in honey and wax after treatment of honey bee colonies with Apivar ® or Asuntol ® 50. Apidologie 38, 534–544
Martin, S.J. (2004) Acaricide (pyrethroid) resistance in Varroa destructor. Bee. World 85, 67–69
Melathopoulos, A.P., Winston, M.L., Whittington, R., Smith, T., Lindberg, C., Mukai, A., Moore, M. (2000) Comparative laboratory toxicity of neem pesticides to honey bees (Hymenoptera: Apidae), their mite parasites Varroa jacobsoni (Acari: Varroidae) and Acarapis woodi (Acari: Tarsonemidae), and brood pathogens Paenibacillus larvae and Ascophaera apis. J. Econ. Entomol. 93, 199–209
Menkissoglu-Spiroudi, U., Diamantidis, G., Georgiou, V.E., Thrasyvoulou, A. (2000) Determination of malathion, coumaphos, and fluvalinate residues in honey by gas chromatography with nitrogen–phosphorus or electron capture detectors. J. AOAC Int. 83, 178–182
Mullin, C.A., Frazier, M., Frazier, J.L., Ashcraft, S., Simonds, R., vanEngelsdorp, D., Pettis, J.S. (2010) High levels of miticides and agrochemicals in North American apiaries: implications for honey bee health. PLoS ONE 5, 1–19
Nasr, M.E., Wallnar, K. (2003) miticides residues in honey and wax in north America. Am. Bee. J. 143, 322
Rial-Otero, R., Gaspar, E.M., Moura, I., Capelo, J.L. (2007) Gas chromatography mass spectrometry determination of acaricides from honey after a new fast ultrasonic-based solid phase micro-extraction sample treatment. Talanta 71, 1906–1914
Rice, N.D., Winston, M.L., Higo, H.A. (2004) Integrated Pest Management for the parasitic mite Varroa destructor (Anderson and Trueman) in colonies of honey bees (Apis mellifera). Am. Bee. J. 144, 791–795
Russo, M.V., Neri, B. (2002) Fluvalinate residues in honey by capillary gas chromatography–electron capture detection–mass spectrometry. Chromatographia 55, 607–610
Thrasyvoulou, A.T., Pappas, N. (1988) Contamination of honey and wax with malathion and coumaphos used against the Varroa mite. J. Apic. Res. 27, 55–61
Thrasyvoulou, A.T., Ifantidis, M.D., Pappas, N.L., Simmons, K. (1985) Malathion residues in Greek honey. Apidologie 16, 89–94
Tomlin, C. (1997) The pesticide manual, a world compendium (7th ed.), British Crop Protection Council, Farnham, UK
Tremolada, P., Bernardinelli, I., Colombo, M., Spreafico, M., Vighi, M. (2004) Coumaphos distribution in the hive ecosystem: case study for modelling applications. Ecotoxicology 13, 589–601
Tsigouri, A.D., Menkissoglu-Spiroudi, U., Thrasyvoulou, A. (2001) Study of tau-fluvalinate persistence in honey. Pest Manag. Sci. 57, 467–471
Tsigouri, A.D., Menkissoglu-Spiroudi, U., Thrasyvoulou, A., Diamantidis, G. (2004) Fluvalinate residues in honey and beeswax after different colony treatments. B. Environ. Contam. Tox. 72, 975–982
Van Buren, N.W.M., Mriën, J., Velthuis, H.H.W., Oudejans, R.C.H.M. (1992) Residues in beeswax and honey of Perizin, an acaricide to combat the mite Varroa jacobsoni Oudemans (Acari: Mesostigmata). Environ. Entomol. 21, 860–865
Waliszewski, S.M., Infanzon, R.M., Carvajal, O., Hart, M.M. (2003) Removing tau-fluvalinate residues from press-extracted honey. J. Sci. Food Agr. 83, 1225–1227
Wallner, K. (1997) The actual beeswax quality in foundations on the market. Apidologie 28, 168–170
Wallner, K. (1999) Varroacides and their residues in bee products. Apidologie 30, 235–248
Westcott, L.C., Winston, M.L. (1999) Chemical acaricides in Apis mellifera (Hymenoptera: Apidae) colonies: do they cause nonlethal effects? Can. Entomol. 131, 363–371
Winston, M.L. (1991) The biology of honey bee. Harvard University Press, UK
Prédire le devenir des pesticides dans la ruche (1° partie): détermination expérimentale des résidus de τ-fluvalinate chez les abeilles, dans le miel et la cire
Fluvalinate / résidus de pesticides / contamination de la cire / contamination du miel / santé de l’abeille
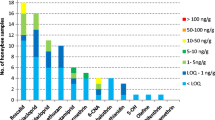
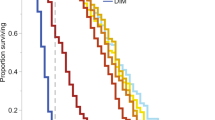
Zusammenfassung – Vorhersage der Verteilung von Pestiziden im Bienenvolk (Teil I): Experimentell bestimmte tau-Fluvalinat-Rückstände in Bienen, Honig und Wachs. Mathematische Modelle werden häufig benutzt, um die Verbreitung von organischen Wirkstoffen in der Umwelt vorherzusagen. Das Bienenvolk kann dabei als Mikro-Ökosystem angesehen werden, in das chemische Kontaminationen von außen und von innen hineinkommen können, je nach Anwendung von Pestiziden zur Bekämpfung von Parasiten. Um die möglichen Kontaminationsebenen von Bienenprodukten vorhersagen zu können, haben wir ein Multi-Kompartment-Modell für das Bienenvolk entwickelt. Um die Validität eines solchen Modells zu überprüfen, sind spezifische Zeitreihenanalysen notwendig. Wir haben daher die Rückstände von tau-Fluvalinat in Bienen, Honig und Wachs in zwei mit Apistan behandelten Bienenvölkern gemessen (Figure 1). Die Rückstände in Bienen wurden über 30 Tage nach der Behandlung verfolgt, bei Honig und Wachs sogar über einen Zeitraum von 180 Tagen (Table I). Im Honig konnten keine Rückstände oberhalb der Nachweisgrenze (2.5 ng g−1) gefunden werden, vermutlich wegen der geringen Wasserlöslichkeit und dem hohen n-Octanol-Wasser-Verteilungskoeffizienten (Log K ow = 4.3) des Wirkstoffes. Die Wirkstoffkonzentrationen in Bienen bewegten sich zwischen 14 und 160 ng g−1 f.w. (Figure 2). Vor der Behandlung waren keine Rückstände in Bienen nachweisbar. Sie stiegen dann bis zum 4. Tag an mit großen Schwankungen zwischen den einzelnen Proben, um dann vom 7. Tag an bis zum Ende der Behandlung (30 Tage) rasch zu einem fast konstanten Niveau (about 50 ng g−1 f.w.) abzusinken. Die Konzentrationen im Wachs lagen zwischen 98 und 1,630 ng g−1 (Figure 2). Im Wachs waren bereits vor der Behandlung Rückstände nachweisbar, vermutlich aufgrund früherer Behandlungen oder der Verwendung von kontaminiertem Material. Die tau-Fluvalinat-Rückstände in Wachs stiegen nach der Behandlung langsam bis zum 60. Tag an und blieben dann bis zum 180. Tag auf einem konstanten Niveau. Unsere Ergebnisse liegen im mittleren Bereich der bisher veröffentlichten Daten anderer Untersuchungen. Das auffälligste Ergebnis unserer Literaturrecherche ist die extrem hohe Schwankungsbreite der Rückstandswerte von ein und demselben Wirkstoff in derselben Matrix (Figure 3). Diese Unterschiede können mehrere Ursachen haben: (a) Unterschiede bei der Probennahme und der Inhomogenität des gesamten Systems (bei unseren Ergebnissen waren Unterschiede bis zum Faktor 2 darauf zurückzuführen); (b) die Zeitdauer nach der Behandlung (unsere Ergebnisse zeigen zeitabhängige Unterschiede bis zum Faktor 10); (c) die Anwendungsmethode (PVC-Streifen vermeiden eine direkte Wachskontamination während das Sprühen des Wirkstoffes diesen direkt auf das Bienenwachs aufbringt); (d) die Anzahl an Behandlungen pro Bienenvolk (da dieser Wirkstoff akkumuliert). Ein Vorhersagemodell kann helfen, die Variabilität solcher empirischer Untersuchungen besser zu verstehen. Es ist daher das Hauptziel unserer Untersuchung, auf der Basis der experimentell gemessenen tau-Fluvalinat-Konzentrationen in Bienen, Honig und Wachs ein Bienenvolkmodell zu entwickeln. Im zweiten Teil dieses Berichtes wird ein solches neues Bienenvolkmodell vorgestellt.
Fluvalinat / Pestizidrückstände / Wachskontamination / Honigkontamination / Bienengesundheit.
Author information
Authors and Affiliations
Corresponding author
Additional information
Manuscript editor: Monique Gauthier
Rights and permissions
About this article
Cite this article
Bonzini, S., Tremolada, P., Bernardinelli, I. et al. Predicting pesticide fate in the hive (part 1): experimentally determined τ-fluvalinate residues in bees, honey and wax. Apidologie 42, 378–390 (2011). https://doi.org/10.1007/s13592-011-0011-2
Received:
Revised:
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/s13592-011-0011-2