Summary
The adsorption of nickel, zinc, and cadmium by goethite was studied at different metal concentrations of 0.5 and 5 μmole/g goethite, reaction times from 2 h to 42 days and temperatures between 5 and 35° C.
The metal amounts adsorbed strongly increase with pH in the range from 4 to 8. The specificity of the heavy metal adsorption by goethite is characterized by the pH of 50% sorption of the total metal content added (pH50). Under the reaction conditions of these experiments pH50-values of 4.9, 5.6, and 5.8 were found for zinc, nickel, and cadmium, respectively. The differences between the pH50-values closely agree with the differences between the pK-values of the first hydrolysis constants of zinc, nickel, and cadmium, thus indicating that trace metal adsorption by the hydroxylated surfaces of iron oxides is strongly affected by the hydroxocomplex formation of trace metals.
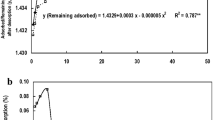
With increasing reaction time and temperature the adsorption of all three metals rises. Besides adsorption at the surface solid state diffusion is also observed which can probably be related to defective structures in the lattice of goethite. Linear plots of the metal amount adsorbed versus the square root of time provide relative diffusion rates for nickel, zinc, and cadmium of 2.47, 1.00, and 0.31, respectively, at 20° C and definite pH. These values show that the effect of diffusion on the binding of metals by goethite is increased in the order Cd <Zn<Ni.
Although goethite is partly dissolved by nitric acid treatment the extraction of metals by this method is incomplete. Considerable metal amounts are still occluded and can only be mobilized by the complete dissolution of goethite with fluoric acid. At the reaction conditions used this strongly bound fraction of zinc, cadmium, and nickel comprises 39.0, 29.0, and 10.5%, respectively, of the total amount of metals added. These different values indicate that the binding strength of the metals investigated decreases in the same order.
The binding of heavy metals by goethite is thus determined by adsorption, diffusion and occlusion depending on pH, reaction time and temperature.
Zusammenfassung
Die Adsorption von Nickel, Zink und Cadmium durch Goethit wurde bei unterschiedlichen Reaktionszeiten von 2 h bis zu 42 Tagen sowie bei Temperaturen von 5 bis 35° C in Abhängigkeit vom pH-Wert untersucht.
Die adsorbierten Metallanteile nehmen bei einem konstanten Metallangebot von 0,5 bzw. 5 μmol/g Goethit mit steigendem pH zwischen 4 und 8 stark zu. Der bei 50%iger Adsorption der angebotenen Metalle gemessene pH-Wert (pH50) kennzeichnet die Spezifität der Schwermetalladsorption durch Goethit. Unter den gewählten Reaktionsbedingungen werden pH50-Werte von Zink, Nickel und Cadmium von 4,9; 5,6 und 5,8 erreicht. Die Unterschiede zwischen den pH50-Werten stimmen dabei mit den Differenzen der pK-Werte der ersten Hydrolysekonstanten dieser Metalle relativ gut überein. Damit wird, wie in der Literatur mehrfach beschrieben, die Bedeutung der Hydroxo-Komplexe für die Adsorption von Schwermetallen an hydroxylierten Oberflächen von Eisenoxiden deutlich.
Mit steigender Reaktionszeit und Temperatur nehmen die adsorbierten Anteile der drei Metalle deutlich zu. Neben einer Adsorption an der Oberfläche der Goethitpartikel findet auch eine Diffusion der Metallionen — vermutlich an Stellen von Gitterfehlordnungen — in das Partikelinnere statt. Mit Hilfe der linearen Beziehungen zwischen der Adsorption und der Quadratwurzel der Reaktionszeit lassen sich relative Diffusionsraten von Nickel, Zink und Cadmium ermitteln, die bei 20°C sowie definiertem pH Werte von 2,47; 1,00 und 0,31 aufweisen. Damit steigt der Einfluß der Diffusion auf die Metalladsorption in der Reihe Cd<Zn<Ni beträchtlich an.
Wie Versuche zur Extrahierbarkeit der durch Goethit gebundenen Metallanteile zeigen, verbleibt trotz teilweiser Auflösung der Goethitpartikel durch Salpetersäure ein beträchtlicher Anteil in okkludierter Form gebunden, der erst nach vollständiger Goethitauflösung durch Flußsäure freigesetzt wird. Dieser Anteil beträgt unter den gewählten Reaktionsbedingungen beim Zink, Cadmium und Nickel 39,0; 29,0 und 10,5 % der insgesamt zugesetzten Metallmenge. Die aufgeführten Restanteile geben gleichzeitig Hinweise zu der in gleicher Reihenfolge abnehmenden Stärke der Bindung zwischen den drei Metallen und Goethit. — Die Bindung der Schwermetalle durch Goethit wird damit insgesamt durch Adsorption, Diffusion und Okklusion in Abhängigkeit von pH, Reaktionszeit und Temperatur bestimmt.
Similar content being viewed by others
Literatur
Jenne EA (1968) Adv Chem Ser 73:337–387
Grimme H (1968) Pflanzenernähr Dung. Bodenk 121:58–65
Forbes EA, Posner AM, Quirk JP (1976) J Soil Sci 27:154–166
Benjamin MM, Leckie JO (1981) J Colloid Interface Sci 79:209–221
Kinniburgh DG, Jackson ML, Syers JK (1976) Soil Sci Soc Am J 40:796–799
Kühnel RA, van Hilten P, Rooda HJ (1975) Clays and Clay Minerals 23:349–354
Sidhu PS, Gilkes RJ, Posner AM (1981) Soil Sci Soc Am J 45:641–644
Soon YK, Bates TE (1982) J Soil Sci 33:477–488
Quirk JP, Posner AM (1975) In: Nicholas DJD, Egan AR (eds) Trace elements in soil — plant — animal systems, pp 95–107. Academic Press Inc, New York
Schwertmann U, Fischer WR (1966) Z Anorg Allg Chem 346:137–142
Tiller KG, Nayyar VK, Clayton PM (1979) Aust J Soil Res 17:17–28
Jurinak JJ, Whitmore JC, Wagenet RJ (1977) Soil Sci Soc Am J 41:721–724
Kinniburg DG, Jackson UL (1982) Soil Sci Soc Am J 46:56–61
Smith RM, Martell AE (1976) Critical stability constants, vol 4: Inorganic complexes. Plenum Press, New York
Tiller KG, Gerth J, Brümmer G (1983) in Vorbereitung
James RO, Healy TW (1972) J Colloid Interface Sci 40:42–52
Brümer G, Tiller KG, Herms U, Clayton PM (1983) Geoderma, im Druck
Author information
Authors and Affiliations
Additional information
Die Verfasser sind Frau S. Kneesch für ihre Hilfe bei der Durchführung der Analysen und für die Anfertigung der Zeichnungen zu herzlichem Dank verpflichtet.
Rights and permissions
About this article
Cite this article
Gerth, J., Brümmer, G. Adsorption und Festlegung von Nickel, Zink und Cadmium durch Goethit (α-FeOOH). Z. Anal. Chem. 316, 616–620 (1983). https://doi.org/10.1007/BF00492275
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00492275