Abstract
The potential of predators to impact the establishment of aphid vectors and the spread of beet yellows virus in sugar beet was examined.
Myzus persicae carrying beet yellows virus (BYV) were released on six interior sites and six edge sites in each of four fields at the end of May. Aphids established at low densities and BYV was spread in circular patches around the infested plants at all sites. The number of diseased plants per patch at the end of September ranged from a field-average of 130 to 210 in the four fields. There was a weak tendency towards better aphid establishment and greater virus spread in fields in less complex landscapes. Edge sites had less virus spread than interior sites in one field, more virus spread in two other fields, and there was no statistically significant difference in the fourth field.
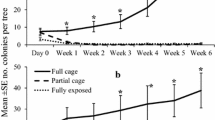
In the field where virus spread was lowest at edge sites, we used predator exclosure and direct observation to manipulate and quantify the effects of early season predation. On a warm day in early June, 81% ofAphis fabae exposed to predators on young beet plants disappeared during a 24 h period, compared to 10% of aphids protected by clipcages. Intermediate levels of predator exclusion, allowing aphids to walk away but restricting predator access, showed that predation was responsible for aphid disappearance.Cantharis lateralis L. (Coleoptera: Cantharidae) was the most frequently observed foliar predator (>90%). It was found eating aphids on several occasions. The incidence of predators was 1.8 per plant per h in the field interior and 3.8 per plant per h. near the edge.
In the same field, aphids and virus were released in six edge and six interior sites, that were surrounded by 0.5 m high plastic open-top barriers (‘exclosures’). Pitfall trapping inside the barriers reduced potential soil predator densities to ca. one-tenth of the open field level and arrivals of flying predators were reduced. Inside the exclosures, aphid establishment was enhanced, and virus spread at exclosure sites was increased by about 50% compared to open sites.
Foliar and pitfall sampling yielded the following predators:Cantharis lateralis, C. rufa L. (Coleoptera: Cantharidae),Coccinella septempunctata L.,C. undecimpunctata L. (Coleoptera: Coccinellidae),Pterostichus cupreus (L.),Harpalus rufipes (de Geer),Patrobus atrorufus (Strom),Trechus quadristriatus (Schrk.),Bembidion lampros (Herbst) (Coleoptera: Carabidae). In a laboratory no-choice trial (with 10M. persicae /day offered), each of these species ate aphids with consumption rates varying from 1.7 to 9.2 aphids/day.
The results show that early predation substantially impacted aphid establishment in one field, and resulted in reduced virus spread. Results in the other fields show that these results cannot be easily generalized.
Résumé
Myzus persicae, porteur du virus de la jaunisse de la betterave a été lâché en six sites à l’intérieur et en six autres sites sur les bordures de chacun des 4 champs étudiés, à la fin mai. Les pucerons se sont installés à de faibles densités et le virus s’est propagé en des taches circulaires autour des plantes infestées de tous les sites. Le nombre de plantes malades par tache, fin septembre, était compris en moyenne par champ entre 130 et 210 pour les quatre parcelles. Il y avait une faible tendance à une meilleure installation des pucerons et une plus grande transmission des virus dans les champs situés dans les paysages les moins complexes. Les sites de bordure présentaient une transmission de virus plus faible que les sites de l’intérieur dans un des champs, davantage de transmission de virus dans deux autres champs et il n’y avait pas de différence significative dans le quatrième.
Dans le champ où la transmission du virus était la plus faible au niveau des sites de bordure, nous avons utilisé une méthode d’exclusion des prédateurs ainsi que l’observation directe dans le but de manipuler et de quantifier les effets de la prédation en début de saison. Au cours d’une journée chaude de début juin, 81% desA. fabae exposés aux prédateurs sur des jeunes plants de betterave ont disparu en 24 heures, comparé à 10% pour les pucerons protégés dans des ‘clips cages’. Des niveaux intermédiaires d’exclusion des prédateurs permettant aux pucerons de partir en marchant mais restreignant l’accès des prédateurs, ont montré que la prédation était responsable de la disparition du puceron.Cantharis lateralis L. (Col., Cantharidae) était le prédateur le plus fréquement observé sur le feuillage (>90%). Il a été trouvé à différentes occasions en train de consommer des pucerons. L’incidence des prédateurs était de 1,8 par plante/heure à l’intérieur de la parcelle et 3,8 par plante/ heure près des bordures. Dans le même champ, des pucerons et du virus ont été déposés dans 6 sites intérieurs et six sites de bordure qui étaient entourés de barrières de plastique de 0,5 m de haut ouvertes à la partie supérieure. Des pièges de Barber placés à l’intérieur de ces barrières réduisaient la densité des prédateurs potentiels à 1/10 du niveau du champ; l’arrivée de prédateurs volant était également réduite. A l’intérieur de ces barrières, l’installation des pucerons était favorisée et la dissémination était augmentée d’environ 50 % par rapport aux sites ouverts.
La collecte sur le feuillage et dans les pièges a permis de capturer les prédateurs suivants :Cantharis lateralis, C. rufa L. (Coleoptera : Cantharidae),Coccinella septempunctata L.,C. undecimnotata L. (Col. : Coccinellidae),Pterostichus cupreus (L.),Harpalus rufipes (de Geer),Patrobus atrorufus (Strom),Trechus quadristriatus (Schrk.),Bembidion lampros (Herbst) (Col. : Carabidae). Dans un essai de laboratoire sans choix (avec 10M. persicae présentés par jour), chacune des espèces précédentes a consommé des pucerons à un rythme variant de 1,7 à 2,2 pucerons /jour. Ces résultats montrent que la prédation précoce a réduit sérieusement l’installation des pucerons dans un champs et a diminué la dissémination du virus. Les résultats des autres champs montrent que ces résultats ne peuvent pas être facilement généralisés.
Similar content being viewed by others
References
Basedow, Th. — 1987. Die Bedeutung von Hecken, Feldrainen und pflanzenschutz-mittelfreien Ackerrandstreifen fiir die Tierwelt derÄcker.Ges. Pfl., 39, 421–429.
Basedow, Th. — 1990. Zum Einfluß von Feldrainen und Hecken auf Blattlausräuber, Blattlausbefall und die Notwendigkeit von Insektizideinsätzen im Zuckerrtibenanbau.Ges. Pfl., 42, 241–245.
Bennett, C. W. — 1960. Sugar beet yellows disease in the United States. —U.S. Dep. Agric. Agric. Res. Serv. Tech. Bull., 1218.
Colunga-Garcia, M., Gage, S. H. & Landis, D. A. — 1997. The response of an assemblage of Coccinellidae (Coleoptera) to a diverse agricultural landscape. —Environ. Entomol. (In press).
de Koeijer, K. J. &van der Werf, W. — 1995. Effect of beet yellowing viruses on light interception and light use efficiency of the sugarbeet crop. —Crop Prot., 14, 291–297.
DuBois, D., Häni, A., Ammon, H. U. &Keller, S. — 1993. Einfluss der Unkrautbekämpfung auf Ertrag und Virusbefall von Zuckerrüben. —Landw. Schweiz, 6, 133–138.
Duelli, P., Studer, M., Marchand, I. &Jakob, S. — 1990. Population Movements of Arthropods between Natural and Cultivated Areas. —Biol. Cons., 54, 193–207.
Galecka, B. — 1966. The Role of Predators in the Reduction of Two Species CF Potato Aphids,Aphis nasturtii Kalt. andA. frangulae Kalt. —Ekol. Polska, Serie A, 16, 245–274.
Hance, Th. — 1986. Experiments on the population control ofAphis fabae by different densities of Carabidae (Coleoptera: Carabidae). —Ann.Soc. R. Zool. Belg. 116, 15–24.
Hance, Th. — 1987. Predation impact of carabids at different population densities onAphis fabae development in sugar beet. —Pedobiology, 30, 251–262.
Hance, Th., Gregoire-Wibo, C. & Lebrun, P. — 1990. Agriculture and ground-beetles populations: the consequences of crop types and surrounding habitats on activities and species composition.Pedobiology, 337–346.
Häni, A., Ammon, H. U. &Keller, S. — 1990. Influence of weed densities on aphid populations and spread of virus yellows in sugar beets. —Landw. Schweiz., 3, 217–221.
Lobner, U. &Hartwig, O. — 1994. Soldier beetles (Col.: Cantharidae) and nabid bugs (Het.: Nabidae) occurrence and importance as aphidophagous predators in winter wheat fields in the surroundings of Halle/Saale (Sachen-Anhalt). —Bull. OILB-SROP, 17, 179–187.
Maredia, K. M., Gage, S. H., Landis, D. A. &Scriber, J.M. — 1992a. Habitat Utilization Patterns by the Seven-Spotted Lady Beetle (Coleoptera: Coccinellidae) in a Diverse Agricultural Landscape. —Biol. Contr., 2, 159–165.
Maredia, K. M., Gage, S. H., Landis, D. A. &Wirth, T. M. — 1992b. Ecological Observations on Predatory Coccinellidae (Coleoptera) in Southwestern Michigan. —Great Lakes Entomol., 25, 265–270.
Smith, H. G. &Hallsworth, P.B. — 1990. The effect of yellowing viruses on yield of sugar beet in field trials, 1985 and 1987. —Ann. Appl. Biol., 116, 503–511.
Tits, M. &Wauters, A. — 1991. Overview of the phytosanitary conditions of sugar beet in 1991. —Parasitica, 47, 63–72.
van Emden, H. F. — 1972. Aphid Technology. —Academic Press, London, 344 pp.
van der Werf, W., Westerman, P.R., Verweij, R. &Peters, D. — 1992. The influence of primary infection date and establishment of vector populations on the spread of yellowing viruses in sugar beet. —Ann. Appl. Biol., 121, 57–74.
van der Werf, W. — 1995. How do immigration rates affect predator/prey interactions in field crops? Predictions from simple models and an example involving the spread of aphid-borne viruses in sugar beet, pp. 295–312. In: Arthropod Natural Enemies in Arable Land I (S. Toft &W. Riedel, eds.), —Acta Jutlandica, vol. 70: 2, Aarhus University Press, Denmark.
Weber, C. A., Godfrey, L. D. &Mauk, P. A. — 1996. Effects of parasitism byLysiphelebus testaceipes (Hymenoptera: Aphidiidae) on transmission of beet yellows closterovirus by bean aphid (Homoptera: Aphididae). —J. Econ. Entomol., 89, 1431–1437.
Wetzel, T., Stark, A., Löbner & Hartwig, O. — On the occurrence and importance of soldier beetles (Coleoptera: Cantharidae) and nabid bugs (Heteroptera: Nabidae) as aphidophagous predators in cereal fields. —Z. Pfl. krakh. Pfl.schutz, 98, 364–370.
Wilkinson, L. — 1989. SYSTAT: The system for statistics, Evanston, IL. SYSTAT Inc.
Wratten, S. D. &Thomas, C. F. G. — 1990. Farm-scale spatial dynamics of predators and parasitoids in agricultural landscapes. pp. 220–235. In: Species Dispersal in Agricultural Habitats (R. G. H. Bunce &D. C. Howard, eds.), —Belhaven Press, London.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Landis, D.A., Van der Werf, W. Early-season predation impacts the establishment of aphids and spread of beet yellows virus in sugar beet. BioControl 42, 499–516 (1997). https://doi.org/10.1007/BF02769810
Received:
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/BF02769810